- KAIST 바이오및뇌공학과 박지호 교수 연구팀, 흡입 치료에 최적화된 mRNA 전달체 개발
- 에어로졸화 과정에서의 안정성과 폐 미세환경 투과에 특화된 입자 조성으로 높은 효율로 폐 내 단백질 발현 가능
- 기존 지질나노입자 대비 26배 이상의 단백질 발현량을 보여 호흡기 바이러스 및 난치성 폐질환의 mRNA 흡입 치료 기대
코로나19의 전 세계적 유행 이후, 폐 등 호흡기 질병에 대비하기 위한 mRNA 백신 및 치료제는 차세대 치료제로 주목받고 있다. 하지만 기존 mRNA 백신용 전달체가 가지고 있는 한계점을 극복하고 KAIST 연구진이 호흡기 바이러스 및 난치성 폐질환의 mRNA 흡입 치료를 가능케 하며 유전자 폐 치료 연구의 근간이 될 연구에 성공했다.
KAIST(총장 이광형)는 바이오및뇌공학과 박지호 교수 연구팀이 유전자 폐 치료에 최적화된 나노 전달체를 개발했다고 7일 밝혔다.
연구팀은 기존 mRNA 전달을 위해 활용되던 지질나노입자(이하 lipid nanoparticle, LNP)의 에어로졸화 과정에서의 불안정성과 폐 미세환경에서의 낮은 전달 효율을 해결하기 위해 이온화성 지질나노복합체(ionizable lipocomplex, iLPX)를 개발했다.
iLPX는 이온화성 리포좀의 외부에 mRNA를 결합한 형태로, 에어로졸화 과정에서 입자의 구조를 유지하기 때문에 흡입 전달에 용이하다. 또한, 폐 미세환경 내에서 폐계면활성제와의 상호작용을 유도해 호흡 운동을 활용, mRNA를 높은 효율로 폐 세포 내로 전달할 수 있다.
흡입 전달 및 폐 미세환경을 고려한 모방 환경 및 마우스 폐에서의 단백질 발현을 토대로 한 다차원 선별 과정을 통해 iLPX의 구성 요소들을 최적화시킴으로써 흡입용 mRNA 전달체(Inhalation optimized-iLPX, 이하 IH-iLPX)를 완성했다.
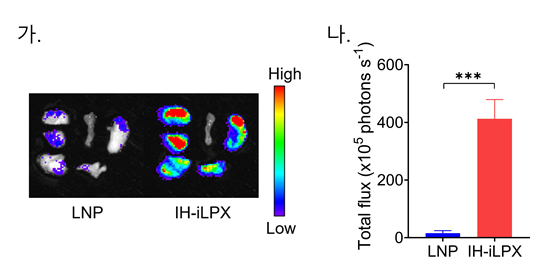
연구팀은 에어로졸화 전후의 입자 크기, 균일도, mRNA 탑재율을 비교함으로써 IH-iLPX의 월등한 에어로졸화 안정성을 증명했다. 나아가, IH-iLPX를 전달한 마우스에서 LNP 전달 마우스보다 26배 높은 단백질 발현이 유도됨을 확인했다.
연구팀은 동물 모델에서 흡입 전달된 IH-iLPX가 폐 특이적으로 단백질을 발현시키며, 폐포 상피세포와 기관지 상피세포에서 mRNA를 효과적으로 전달함을 확인했다. 또한 혈액 생화학 분석과 조직 검사를 토대로 IH-iLPX가 폐와 혈액 환경에서 독성이 없음을 확인했기 때문에 효과적인 폐내 mRNA 발현뿐만 아니라 생체 안전성 측면에서 큰 의의를 갖는다고 밝혔다.
박 교수는 “mRNA를 반드시 내부에 탑재해야 한다는 고정 관념을 깨고 새로운 구성의 입자를 제시함으로써 기존에 불가능했던 흡입형 유전자 치료의 길을 열었다”며 “본 연구실에서 개발한 흡입형 유전자 전달체는 치료 단백질을 암호화하는 mRNA를 탑재해 폐질환에 적용되어 유전자 폐 치료의 적용 범위를 넓힐 것으로 기대된다”이라고 말했다.
KAIST 바이오및뇌공학과 장민철 박사과정이 제1 저자로 참여한 이번 연구 결과는 나노기술 분야 국제학술지 ‘ACS 나노(Nano)’ 9월 3일 자 18권 35호에 게재됐다. (논문명: Inhalable mRNA Nanoparticle with Enhanced Nebulization Stability and Pulmonary Microenvironment Infilration)
이번 연구는 한국연구재단의 중견연구자지원사업의 지원을 받아 수행됐다.
□ 연구개요
mRNA 치료제는 생체적합성과 개발 단계에서의 경제적 이점으로 인해 차세대 치료제로써 주목받고 있다. 특히, COVID-19의 전세계적 유행 이후 호흡기 질병에 대한 mRNA 치료제 개발의 중요성이 강조되었다. 폐 특이적 약물 전달 효율을 높여 부작용을 줄이기 위한 폐 국소적 약물 주입법 중 네뷸라이저를 활용한 흡입 전달법은 비침습적이고, 빠른 흡수가 가능하다는 장점이 있어 호흡기 치료제의 주요 전달법으로 활용되었다. mRNA 기반 흡입 전달 치료제는 감염성 질환뿐만 아니라 천식, 낭포성 섬유증, 특발성 폐섬유증 등 유전자 치료를 필요로 하는 다양한 난치성 질환에 적용될 수 있어, 흡입 전달 기반 mRNA 치료제의 개발이 필요하다.
mRNA 치료제의 전달체로써 상용화된 이온화성 지질을 활용한 LNP는 정맥 주사 후 혈액 내에서 입자 표면의 폴리에틸렌글리콜과 혈청 단백질 간의 교체가 일어나 세포 내로 mRNA를 전달한다. 하지만, 지질나노입자는 흡입 전달하는 경우 에어로졸화 과정에서의 전단력에 의한 입자 구조 파괴, 폐상피세포와 공기의 계면에 존재하는 폐계면활성제에 대한 미미한 투과율, 그리고 낮은 혈청 단백질 환경에서 세포내 전달율이 현저히 떨어지는 등의 뚜렷한 한계점이 존재한다. 현재 임상적으로 사용되고 있는 흡입 전달용 mRNA 치료제는 전무하며, 따라서 기존 mRNA 치료제 흡입전달의 한계점을 극복할 수 있는 mRNA 전달체에 대한 연구가 필요한 상황이다.
본 연구진은 흡입 전달법을 활용한 mRNA 치료제에 사용될 수 있는 흡입 전달용 mRNA 전달 플랫폼을 개발하고 해당 입자 플랫폼을 폐 모방 환경에서 최적화하여 흡입 전달 최적화 나노입자를 개발했다. 개발된 입자는 에어로졸화 과정의 전단력을 견디고, 생체 내에서 폐계면활성제를 투과하며, 낮은 혈청 단백질을 가지는 폐포액 환경에서 세포 내로 잘 전달되어 높은 mRNA 전달 및 단백질 발현 효과를 보였다.

본 기사는 네티즌에 의해 작성되었거나 기관에서 작성된 보도자료로, BRIC의 입장이 아님을 밝힙니다. 또한 내용 중 개인에게 중요하다고 생각되는 부분은 사실확인을 꼭 하시기 바랍니다.
[기사 오류 신고하기]
BRIC(ibric.org) Bio통신원(KAIST) 등록 2024.10.07